|
|
Главная / Наш факультет / Кафедры / Кафедра ФБР
|
Группа рецепции и трансдукции гормональных и метаболических сигналов |
|
|
Состав: проф., зав. лаборатории фотосинтеза, д.б.н. Шишова М.Ф., доц., к.б.н. Маслов Ю.И., ст. преп., к.б.н. Тараховская Е.Р., асс. Кирпичникова А.А., м.н.с. Пузанский Р.К., аспирант Еремина М.А., студенты магистратуры: Прокопьева Ю.П., Киселева А.А., Чень Тинджо, инж. Шевцов Ю.И., Соболь Л.С.
Научная тема:
Рост и развитие растений протекает под действием многообразных факторов, большая часть которых при превышении порогового значения становится стрессовым. Точность идентификации сигнала и быстрое формирование адаптационного ответа лежит в основе жизнеспособности любого организма, определяет последовательность запуска морфогенетических программ, реализуемых как на клеточном, так и на организменном уровнях.
Исследования проводятся по следующим направлениям:
|
|
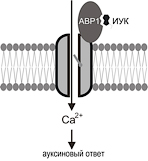
Рис. 1. Модель рецептора ауксина на плазмалемме растительных клеток.
|
Исследование рецепции и первичной трансдукции ауксинового сигнала
Фитогормон ауксин – один из важнейших регуляторов роста растений. Многообразие его действия на клетки определяется наряду с многокомпонентыми системами синтеза, конъюгирования, распада и транспорта гормона, рецепторными системами, трансдукционными путями, активностью ферментов-мишеней и совокупностью гормон-активируемых генов. Выявленный в 2005 г. цитоплазматический рецептор TIR1 и ряд его гомологов приводит к быстрой активации ауксин-индуцируемых генов. Тем не менее, с 80х годов накапливается все больше данные о возможности и необходимости рецепции ауксинового сигнала на наружной поверхности клетки (серия работ группы E.Barbier-Brigoo).
Данный тип рецепции связан с ABP1 – ауксин-связывающим белком, ассоциированным с плазмалеммой при осуществлении рецепторной функции.
|
|
Следует подчеркнуть, что делеция ABP1 гена приводит к летальности у арабидопсиса уже на очень ранних стадиях эмбрионального развития (Chen et al., 2001). На различных модельных объектах было показано, что увеличение содержания ABP1 приводит к интенсификации процесса роста растяжением (Chen et al., 2001, Chen 2001). К сожалению, вопрос идентификации рецептора ауксина на плазмалемме до сих пор остается открытым, так как ABP1 выполняет лишь роль ассоциированного домена рецептора, связываясь с гипотетическим трансмембранным доменом, функция которого заключается в передаче сигнала внутрь клетки. Исследования, проводимые в нашей группе на субклеточном (с использованием изолированной фракции плазмалеммы) и клеточном (протопласты растительных клеток и клеточные линии) уровнях позволили предложить модель ауксинового рецептора – Са2+-канала (рис. 1, Шишова, 1999).
Доказано, что ауксин-индуцируемое повышение цитоплазматической концентрации ионов Са2+ представляет собой первичный этап трансдукции гормонального сигнала. В настоящее время это направление исследований продолжается с использованием моделей с измененной чувствительностью к ауксину (трансгенные линии клеток табака с пониженным содержанием АВР1, мутанты по ABP1 и TIR1, а также клетки, находящиеся на различных этапах роста растяжением).
В работе принимают участие: Шишова М.Ф., Кирпичникова А.А., Еремина М.А. Работа проводится в сотрудничестве с проф. S. Lindberg (Университет Стокгольма, Швеция) и проф. R. Napier (Университет Варвика, Ковентри, Великобритания).
В настоящее время планируется получить растения и клеточные линии, экспрессирующие белковый сенсор Са2+, для дальнейшей компартментализации Са2+ сигнала при действии ауксина.
Идентификация тканеспецифичной экспрессии генов раннего ответа
Последние десятилетия предоставили достаточное количество доказательств регуляции ауксином генов, увеличение экспрессии которых может быть зарегистрировано уже через 5-15 мин после начала воздействия ауксина (Abel, Theologis, 1996; Guilfoyle, 1999; Hagen, Guilfoyle, 2002). Эти гены, активация которых протекает без участия ауксин-индуцированного синтеза белков, принято относить к группе ранних генов или группе первичного ответа. К их числу можно причислить гены таких семейств как Aux/IAAs, SAURs и GH3s. Интенсивность накопления продуктов экспрессии ранних ауксин-идуцируемых генов семейств Aux/IAA, SAUR, ARF и GH3 проанализирован нами в побегах и корнях проростков арабидопсиса с использованием специально разработанных биочипов и метода ДНК-чип-технологии.
Часовое воздействие фитогормона усиливало экспрессию тестируемых генов GH3 во всем проростке. Орган-специфичное изменение экспрессии было показано для генов семейств Aux/IAA, SAUR, и генов, кодирующих транскрипционные факторы и белки трансдукционного каскада, но не относящихся к перечисленным семействам. Незначительное, близкое к пороговому, увеличение экспрессии выявлено для большинства генов ARF в побегах. Воздействие фитогормона (15, 30 и 60 мин) приводило в корнях к устойчивому усилению экспрессии генов IAA1, IAA3, IAA5, IAA11, IAA19, а также GH3-1, GH3-3, GH3-5. Увеличение экспрессии SAUR9 и SAUR10 было меньшим по амплитуде и наблюдалось только на 30 минуте воздействия гормона.
В настоящее время проводятся исследования по определению значимости фосфолипазы А2 в регуляции экспрессии генов раннего ауксинового ответа. Работа выполнена Шишовой М.Ф. в ходе научной стажировки в сотрудничестве с проф. G.Scherer (Университет Ганновера, Германия).
|
|

Рис. 2. Интенсивность флуоресценции образца при определении Cyanine 3 (слева), при определении Cyanine 5 (в центре) и суммарно (справа).
|
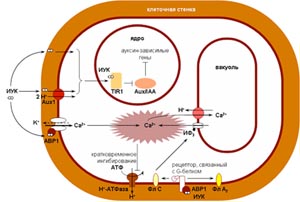
Рис. 3. Схема первичной трансдукции ауксинового сигнала.
|
Выявление значимости Н+-АТФазы плазмалеммы в первичной трансдукции ауксинового сигнала и последующей реализации роста растяжением
Хорошо известно, что изменение рН цитоплазмы является мощнейшим регулятором ферментных систем клетки. Поддержание цитоплазматической концентрации протонов активно, с затратой метаболической энергии, поддерживается посредством Н+-АТФаз плазмалеммы и тонопласта, а также вакуолярной пирофосфатазы. В связи с этим ионы водорода принято рассматривать в качестве вторичного посредника. Наши исследования, согласуясь с рядом данных зарубежных авторов (Felle et al., 1986; Felle, 1988; Gering et al., 1990), показали, что внесение ауксина приводит к быстрому понижению рН цитоплазмы. При использовании ингибиторного анализа доказано, что ауксин-индуцируемое закисление запускается увеличением содержания ионов Са2+ в цитоплазме под действием фитогормона. Предложена схема первичной трансдукции ауксинового сигнала, согласно которой в первые минуты ауксин индуцирует кратковременное ингибирование Н+-АТФазы плазмалеммы, что вызывает деполяризацию и приводит к быстрому изменению направленности ионных потоков (Рис. 3).
|
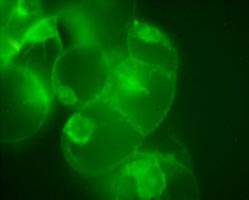
Рис. 4. Клетки суспензионной культуры табака By-2, загруженные Са2+-зависимым флуоресцентным зондом Fura-2.
| 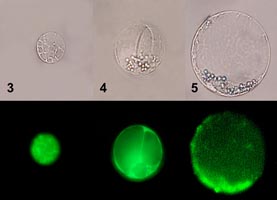
Рис. 5. Клетки суспензионной культуры табака By-2, загруженные рН-чувствительным флуоресцентным зондом BCECF.
|
Наряду с этим считается доказанным, что механизм действия ауксина в инициации роста растяжением заключается в активации Н+-АТФазы плазмалеммы (Hager et al., 1982; Полевой, 1986; Hager, 2003). В связи с этим особое значение приобретает изучение свойств фермента в ходе онтогенеза, в первую очередь в ходе роста растяжением. На модельных объектах: колеоптилях кукурузы и клеточных линиях табака, сохраняющих стадию роста растяжением, проведен анализ гидролитической и транспортной активности фермента. Показано нелинейное изменение интенсивности гидролиза АТФ и транспорта протонов, а также изменение чувствительности Н+-АТФазы плазмалеммы к ванадату и величины Кm фермента.
В работе принимали участие Шишова М.Ф., Кирпичникова А.А., Еремина М.А.
|
|
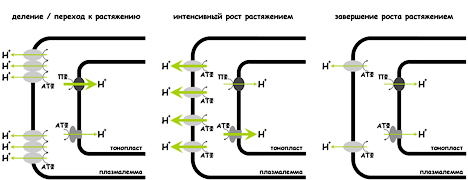
Рис. 6. Модель изменения активности протонных насосов растительной клетки при переходе от деления к растяжению и последующему завершению роста.
|
Совместно со ст.н.с. Танкелюн О.В. проведен сравнительный анализ активности тонопластных Н+-АТФазы и пирофосфатазы тонопласта клеток суспензионной культуры табака. Предложена модель изменения активности протонных насосов растительной клетки при переходе от деления к растяжению и последующему завершению роста (Рис. 6).
|
Выявленное увеличение активности Н+-АТФазы плазмалеммы может быть опосредовано увеличением числа фермента посредством усиления экспрессии кодирующих его генов, а также изменением его свойств в результате пост-трансляционной регуляции. В настоящее время проводится исследование изменения числа ферментативных комплексов на плазмалемме с помощью блот-анализа. В сотрудничестве с группой Лутовой Л.А. (кафедра генетики и селекции СПбГУ) проводится анализ экспрессии генов, кодирующих Н+-АТФазы и пирофосфатазу в клетках гипокотилей и корней проростков арабидопсиса.
Идентификация генов, кодирующих ферменты синтеза, а также белки-транспортеры ауксина у бурой водоросли Fucus vesiculosus
Влияние ауксина на рост и развитие водорослей, в целом, соответствует спектру его физиологического действия у высших растений (Тараховская и др., 2007). Ауксин стимулирует ризоидообразование у ряда видов водорослей, подобно тому, как это происходит у мхов (Basu et al., 2002). В клетках Chara globularis (Charophyta) при обработке ауксином происходят такие же изменения цитоскелета, как и у покрытосеменных растений (Jin et al., 2008). В апикальных и интеркалярных зонах таллома красной водоросли Grateloupia dichotoma ауксин стимулирует деление и растяжение клеток и/или подавляет ветвление, что также напоминает процессы, характерные для покрытосеменных (Yokoya et al., 1996). Действием ауксина определяется поляризация зигот фукоидных водорослей, что подтверждается нарушением нормального развития зигот в присутствии ингибиторов полярного транспорта ИУК (Полевой и др., 2003). К сожалению, представления о ферментах, участвующих в синтезе гормонов у водорослей весьма ограничены. Еще более фрагментарны данные о генах, кодирующих ферменты синтеза фитогормонов в этой группе фотоавтотрофов. Современные данные о геномах и протеомах ряда водорослей позволяют выявить последовательности ДНК, предположительно кодирующие ферменты синтеза или аминокислотные последовательности, имеющие гомологию с консервативными доменами соответствующих ферментов. В связи с этим в 2010 г. начались исследования по идентификации генов, кодирующих ферменты синтеза ауксина у бурой водоросли F.vesiculosus, а также генов, кодирующих транспортеры фитогормона.
В работе принимают участие Шишова М.Ф., Тараховская Е.Р., Маслов Ю.И., Киселева А.П.
Выявление сигнальной функции сахаров и органических кислот в регуляции развития зеленой водоросли Chlamydomonas reinchardtii
Скорость размножения микроводорослей связана как с активностью фотоассимиляционного аппарата, так и со способностью метаболизировать экзогенные органические соединения. С изменением скорости роста культуры связаны изменения метаболизма – соотношения направленности процессов ассимиляции и диссимиляции, что определяет характер накопления тех или иных метаболитов (Heyfets et al., 2000; Yang et al., 2000). Однако энергетические и сигнальные механизмы микроводорослей, обеспечивающие переход к миксотрофии, остаются не до конца ясными. К числу мощнейших трофических сигналов можно в первую очередь отнести сахара. Выявление пула сахаров и других органических соединений, а также их перераспределение между цитоплазмой и хлоропластом с помощью жидкостной и газовой хроматографии, сопряженной масс-спектрометрией является необходимым этапом в исследовании данной проблемы. В связи с расшифровкой генома C. reinhardtii становятся возможными исследования на молекулярно-биологическом уровне. В 2010 г. начаты исследования по выявлению изменений метаболического спектра C. reinhardtii дикого типа и с дефектами синтеза пигментов при автотрофных и миксотрофных типах питания. Планируется получить мутанты с дефектами транспортеров сахаров на плазмалемме и хлоропластных мембранах и оценить их роль в регуляции развития водоросли и как сенсоров метаболических сигналов.
В работе принимают участие Шишова М.Ф., Шаварда А.Л., Маслов Ю.И., Пузанский Р.К. Работа проводится в сотрудничестве с группой проф. Ермиловой Е.В. (кафедра микробиологии СПбГУ) и ст.н.с. Чекуновой Е.М. (кафедра генетики и селекции).
Основные темы исследований, предлагаемые студентам и аспирантам для работы в группе «Физиология стресса и адаптации растений»:
• Выяснение внутриклеточной компартментализации Са2+ и протонного трансдукционных каскадов при восприятии ауксинового сигнала.
• Анализ экспрессии генов, кодирующих Н+-АТФазы и пирофосфатазу в клеточных культурах и нативных органах растений в ходе роста растяжением.
• Идентификация генов, кодирующих ферменты синтеза ауксина у бурой водоросли Fucus vesiculosus, а также генов, кодирующих транспортеры фитогормона.
• Выявление изменений метаболического спектра Chlamydomonas reinhardtii дикого типа и с дефектами синтеза пигментов при автотрофных и миксотрофных типах питания.
• Оценка роли транспортеров сахаров на плазмалемме и хлоропластных мембранах C. reinhardtii в регуляции развития водоросли и как сенсоров метаболических сигналов.
Исследования ведутся с использованием
• спектрофлуориметрических методов оценки концентрации ионов кальция и протона, а также мембранного потенциала, генерируемого на мембранах везикул плазмалеммы;
• метода флуоресцентной микроскопии для оценки внутриклеточной концентрации вторичных посредников;
• спектрофотометрические методов оценки активности ферментов, в том числе их кинетических свойств (Km);
• методов белкового анализа, включая блот-анализ;
• методов ПЦР и ПЦР в реальном времени;
• газовой хроматографии, сопряженной с масс-спектрометрией.
Модельные объекты, используемые в работе:
• проростки арабидопсиса дикого типа, мутанты и трансформанты с измененной чувствительностью к ауксину и нарушенным кодированием протонных транспортеров;
• клеточные линии табака VBI-0 и By-2, дикого типа и антисенс-трансформанты по белку ABP1 (NAS-1).
• бурая водоросль Fucus vesiculosus
• зеленая водоросль Chlamydomonas reinchardtii
Сотрудничество с другими организациями:
Научные группы кафедр генетики и селекции, а также микробиологии биолого-почвенного факультета СПбГУ
Научные учреждения Санкт-Петербурга (Ботанический институт РАН), России (Институт биохимии и генетики, Институт биологии Уфимского НЦ РАН) и зарубежных стран (университеты Гановера, Стокгольма, Варвика, Хельсинки, Институт экспериментальной ботаники Чешской академии наук).
Реализация научных проектов неоднократно финансировалась российскими и международными научными фондами, в том числе из средств СПбГУ:
РФФИ 98-04-49878-а Исследование динамики эндогенной компетентности растительных клеток к ауксину (1998-1999) Руководитель – Шишова М.Ф.
Грант INCO-Copernicus PL №97117 (1998-2004) Руководитель – Полевой В.В. (1998-2001) Руководитель – Шишова М.Ф. c 2001 года
РФФИ 00-04-48551-а Исследование изменения чувствительности растительных клеток к ауксину в онтогенезе (2000-2002) Руководитель – Шишова М.Ф.
РФФИ 00-15-99358-м Мембранный механизм действия ауксина (2000-2001) Руководитель – Шишова М.Ф.
РФФИ 03-04-48167-а Исследование изменения компетентности растительных клеток к ауксину при переходе от деления к растяжению (2003-2005) Руководитель – Шишова М.Ф.
РНП.2.2.2.3. Совместная программа «Михаил Ломоносов II» Министерства образования и науки РФ и DAAD: стажировка в Германии «Роль фосфолипазы А в трансдукции сигналов в растительной клетке» (2006) Руководитель – Шишова М.Ф.
Грант Шведского института (Swedish Institute, 2006-2007) № 01716/ 2005. Роль ионов Са2+ в первичной трансдукции внешних и внутренних сигналов в растительных клетках (The role of Ca2+ in the primary transduction of internal and external signals by plant cells). Руководитель- проф. Sylvia Lindberg (Швеция), координатор проекта в России – Шишова М.Ф.
РФФИ 07-04-01056-а Изменение значимости протонных насосов различных компартментов растительной клетки в процессе роста растяжением (2007-2009) Руководитель – Шишова М.Ф.
РНП.2.2.2.3.16191 Совместная программа «Михаил Ломоносов II» Министерства образования и науки РФ и DAAD: стажировка в Германии «Роль фосфолипазы А в трансдукции ауксинового сигнала» (2008) Руководитель – Шишова М.Ф.
РФФИ 10-04-01035-а Сравнительный анализ активности протонных насосов растительной клетки и характера экспрессии генов, их кодирующих, в процессе роста растяжением (2010-2012) Руководитель – Шишова М.Ф.
НИР СПбГУ 1.38.67.2011 Выяснение молекулярных механизмов, вовлеченных в реализацию метаболического и гормонального контроля роста и дифференцировки растений (2011-2013). Руководитель – Шишова М.Ф.
Шишова М.Ф., Танкелюн О.В., Емельянов В.В., Полевой В.В. Рецепция и трансдукция сигналов у растений. СПб., изд-во СПбГУ, 2008. 266с. ISBN 978-5-288-04882-1
Юрков А., Шишова М., Семенов Д. Особенности развития люцерны хмелевидной с эндомикоризным грибом. Saarbrücken, LAP Lambert Academic Publishing, 2010. 214с. ISBN 978-3-8433-0360-6
Ермилова Е.В., Залуцкая Ж.М., Лапина Т.В., Шишова М.Ф. Количественный анализ экспрессии генов. СПб., Тесса, 2011. 121с. ISBN 978-5-94086-079-2
Статьи в научных журналах и сборниках:
Шишова М.Ф., Опперман К., Пахлер М., Шталь Ф., Шерер Г. Орган-специфичная экспрессия ранних ауксин-зависимых генов проростков арабидопсиса. // Вестник С.-Петербургского ун-та. Сер. 3. 2011. Вып. 3. С. 89-100.
Пузанский Р.К., Тараховская Е.Р., Маслов Ю.И., Шишова М.Ф. Влияние экзогенных органических веществ и освещенности на рост микроводорослей. // Вестник С.-Петербургского ун-та. Сер. 3. 2011. Вып. 2. С. 85-99.
Рудашевская Е.Л., Яковлев А.Ю., Яковлева О.В., Шишова М.Ф. Цитохимическое выявление активности Н+-АТФазы плазмалеммы и ее изменения у клеток колеоптилей проростков кукурузы разного возраста. // Цитология. 2009. Т. 51, № 2. С. 149-154.
Тараховская Е.Р., Маслов Ю.И., Шишова М.Ф. Фитогормоны водорослей. // Физиология растений. 2007. Т. 54, № 2. С. 186-194.
Кирпичникова А.А., Рудашевская Е.Л., Михайлова Ю.В., Шишова М.Ф. Получение везикулярной фракции плазмалеммы из клеток каллусной культуры табака VBI-0 и анализ ее АТФазной активности. // Вестник С.-Петербургского ун-та. Сер. 3. 2005. Вып. 4. С. 62-75.
Shishova M., Lindberg S. Auxin perception and plasma membrane Ca2+-channels. // Intracellular Signaling in Plant and Animal Systems. / eds. M. Kravetch. Kiev, 2004. P. 268-281.
Рудашевская Е.Л., Кирпичникова А.А., Шишова М.Ф. Активность Н+-АТФазы везикулярных фракций плазмалеммы, очищенных двумя методами, в присутствии бридж 58. // Вестник С.-Петербургского ун-та. Сер. 3. 2004. Вып. 2. С. 111-118.
Рудашевская Е.Л., Емельянов В.В., Кирпичникова А.А., Бурова Е.А., Бобинова О.А., Шишова М.Ф. Зависимость возрастных изменений ростовой активности колеоптилей и мезокотилей кукурузы от содержания индолил-3-уксусной кислоты. // Вестник С.-Петербургского ун-та. Сер. 3. 2002. Вып. 3. С. 99-106.
Шишова М.Ф., Рудашевская Е.Л., Инге-Вечтомова Н.И., Кирпичникова А.А., Москалева О.В., Выхвалов К.А. Изменение ауксин-индуцированных реакций в зависимости от возраста проростков кукурузы. // Вестник С.-Петербургского ун-та. Сер. 3. 2001. Вып. 1, (№ 3). С. 50-56.
Shishova M., Lindberg S. Auxin-Induced cytosolic acidification in wheat leaf protoplasts depends on external concentration of Ca2+. // Journal of Plant Physiology. 1999. V. 46, N 5. P. 190-196.
Шишова М.Ф., Линдберг С., Полевой В.В. Активация ауксином транспорта Ca2+ через плазмалемму растительных клеток. // Физиология растений. 1999. Т. 46, №5. С. 718-727.
Шишова М.Ф., Рудашевская Е.Л., Инге-Вечтомова Н.И., Глинкина М.В., Кирпичникова А.А., Выхвалов К.А. Свойства катионных каналов плазмалеммы клеток колеоптилей кукурузы, активируемых ауксином. // Вестник С.-Петербургского ун-та. Сер. 3. 1999. Вып. 3. С. 36-43.
Шишова М.Ф., Инге-Вечтомова Н.И., Рудашевская Е.Л., Выхвалов К.А. Прямое действие ауксина на транспорт ионов кальция через плазмалемму растительных клеток. // Вестник С.-Петербургского ун-та. Сер. 3. 1998. Вып. 2. С. 89-96.
Шишова М.Ф., Инге-Вечтомова Н.И., Выхвалов К.А., Рудашевская Е.Л., Полевой В.В. Ауксин-зависимый транспорт ионов K+ и Ca2+ через мембрану везикул плазмалеммы клеток колеоптилей кукурузы. // Физиология растений. 1998. Т. 45, №1. С. 79-85.
Шишова М.Ф., Инге-Вечтомова Н.И., Рудашевская Е.Л., Полевой В.В. Действие ауксина на транспорт катионов через мембрану везикул плазмалеммы клеток колеоптилей кукурузы. // Доклады РАН. 1997. Т. 356, № 5. С. 700-704.
Polevoi V.V., Sinyutina N.F., Salamatova T.S., Inge-Vechtomova N.I., Tankelyun O.V., Sharova E.I., Shishova M.F. Mechanism of auxin action: Second messengers. // Plant Hormone Signal Perception and Transduction. / eds. A.R. Smith, A.W. Berry, N.V.J. Harpham et. al. Kluwer Academic Publishers, the Netherlands. 1996. P. 223-231. ISBN 0-7923-3768-9.
Шишова М.Ф., Полевой В.В. Влияние импульсного действия ауксина на биоэлектрическую реакцию отрезков колеоптилей кукурузы. // Вестник С.-Петербургского ун-та. Сер. 3. 1993. Вып. 3. С. 83-87.
Инге-Вечтомова Н.И., Щипарев С.М., Калинин В.Д., Шишова М.Ф., Выхвалов К.А. Изучение пассивного и активного транспорта ионов через плазмалемму клеток колеоптилей кукурузы с помощью флуоресцентных зондов. // Физиология и биохимия культурных растений. 1993. Т. 25, №2. С. 119-126.
Шишова М.Ф., Полевой В.В. Ауксин-зависимая биоэлектрическая реакция и транспорт ИУК в отрезках проростков кукурузы. // Вестник С.-Петербургского ун-та. Сер. 3. 1992. Вып. 2. С. 85-91.
|
|
|
 |
|

|
|
|
|
199034, Санкт-Петербург,
Университетская наб. 7/9
Тел.: + 7 (812) 328-96-95
Заведующий кафедрой
д.б.н., проф. Сергей Семенович Медведев
|
e-mail:
|
s.medvedev@spbu.ru
|
Секретарь
к.б.н., доц. Наталия Глебовна Осмоловская
|
e-mail:
|
n.osmolovskaya@spbu.ru
|
|
|
